Inhaltsverzeichnis
Wichtigste Erkenntnisse
- Cannabis ist keine anerkannte Therapie gegen COVID-19 und ersetzt keine leitliniengestützte Behandlung.
- Einzelne Cannabinoide wie CBDA, CBGA, CBG und CBL zeigten in Laborversuchen interessante antivirale Effekte – bisher jedoch ohne klinischen Wirksamkeitsnachweis am Menschen.
- CBD wurde in einer hochwertigen klinischen Studie bei leichtem bis mittelschwerem COVID-19 untersucht, ohne eindeutig positives Ergebnis.
- Für Long COVID liefern erste Pilotstudien Hinweise auf gute Verträglichkeit – einen Wirksamkeitsnachweis erbringen sie nicht.
- CBD-Produkte aus dem Handel sind in Deutschland keine Arzneimittel. Sie unterscheiden sich grundlegend von den standardisierten Reinsubstanzen, die in Studien eingesetzt werden. Übertragungen von Studienergebnissen auf frei käufliche Produkte sind daher nicht zulässig.
- Wechselwirkungen mit bestimmten Medikamenten und die Belastung der Atemwege durch das Rauchen von Cannabis sind relevante Punkte, die man kennen sollte.
Hol dir dein Cannabis Rezept schon ab 9,95 €
Ärzte sind gerade online
Die Frage, ob Cannabinoide, die Wirkstoffe aus der Cannabispflanze, bei COVID-19 eine Rolle spielen könnten, weckt unter Wissenschaftlern und Forschern seit dem Beginn der Pandemie wachsendes Interesse. Es gibt mittlerweile eine Reihe von Laborstudien mit interessanten Ergebnissen. Klinische Studien mit echten Patientinnen und Patienten sind dagegen noch rar.
Dieser Artikel gibt dir einen sachlichen Überblick über die aktuellen Entwicklungen in der Forschung, wo sie noch Lücken hat und was das für dich als Leserin oder Leser bedeutet (1,2).
Was sagt die Forschung: Cannabinoide und COVID-19
Nach aktuellem Wissenstand gilt Cannabis nicht als bewiesene oder empfohlene Behandlung gegen COVID-19. Was die Forschung bisher zeigt:
- Bestimmte Cannabinoide entfalten im Labor antivirale und entzündungshemmende Effekte. Ob diese Ergebnisse auf die Situation beim Menschen übertragbar sind, ist bisher nicht ausreichend belegt (1,3,4).
- Für die medizinische Praxis bedeutet das: Impfung, frühe antivirale Therapie bei Risikogruppen sowie eine leitliniengemäße Behandlung schwerer Verläufe bleiben der Standard.
- Cannabinoide tauchen in den aktuellen Behandlungsempfehlungen der Weltgesundheitsorganisation (WHO) und der US-amerikanischen Infektionskrankheiten-Gesellschaft (IDSA) nicht als empfohlene COVID-19-Therapie auf (3,4).
Den entscheidenden Unterschied sollte man immer im Kopf behalten: Zwischen einem interessanten Laborbefund und einem klinisch bewiesenen Nutzen beim Menschen liegt ein sehr großer Schritt. Genau dieser Schritt ist bei Cannabinoiden gegen COVID-19 bislang noch nicht überzeugend vollzogen worden. Das macht die bisherigen Ergebnisse nicht wertlos – ordnet sie aber richtig ein (1,2,5).
Wie wirken Cannabinoide biologisch und was wird erforscht?
Grundsätzlich kommen zwei Wege infrage, auf denen Cannabinoide theoretisch wirken könnten: ein direkter Effekt auf das Virus selbst und ein indirekter Effekt über Entzündungsprozesse im Körper. Beides ist biologisch plausibel und wird durch Zell- und Tierversuche gestützt – aber eben noch nicht durch Studien am Menschen bestätigt (6,7,8,9).
Eine wichtige Grundlage dafür ist das sogenannte Endocannabinoid-System (ECS). Einfach erklärt: Unser Körper hat von Natur aus Andockstellen für Cannabinoide – sogenannte Rezeptoren. Eine bestimmte Art davon, die CB2-Rezeptoren, sitzt auf vielen Immunzellen und ist an der Steuerung von Entzündungsreaktionen beteiligt. Das erklärt biologisch, warum Cannabinoide überhaupt mit dem Immunsystem in Wechselwirkung treten können.
Wie könnten Cannabinoide das SARS-CoV-2-Virus direkt beeinflussen?
- In einer viel beachteten Laborstudie zeigten CBDA (Cannabidiolsäure) und CBGA (Cannabigerolsäure) – beides Vorstufen der bekannteren Stoffe CBD und CBG – die Fähigkeit, an das sogenannte Spike-Protein von SARS-CoV-2 und der Beta-Variante zu binden (6).
- Das Spike-Protein ist der Teil des Virus, mit dem er in Körperzellen eindringt. Er dockt dabei an einen bestimmten Empfänger auf der Zelloberfläche an, den sogenannten ACE2-Rezeptor.
- Wenn Cannabinoide diese Andockstelle blockieren würden, könnte der Virus theoretisch schlechter in die Zelle gelangen. Bisher ist das jedoch nur im Labor beobachtet worden, nicht beim Menschen.
- Für CBD selbst beschrieb eine weitere Arbeit, dass es die Vermehrung des Virus in Zellkulturen und in Tierversuchen hemmen kann – unter anderem, indem es die körpereigene antivirale Abwehrantwort (sogenannte Interferone, also Botenstoffe des Immunsystems) aktiviert (7).
- Neuere Laborversuche legen außerdem nahe, dass CBG (Cannabigerol) und CBL (Cannabicyclol) einen späteren Schritt der Infektion stören könnten, nämlich die sogenannte Zellfusion – also den Moment, in dem der Virus mit der Zellmembran verschmilzt (9).
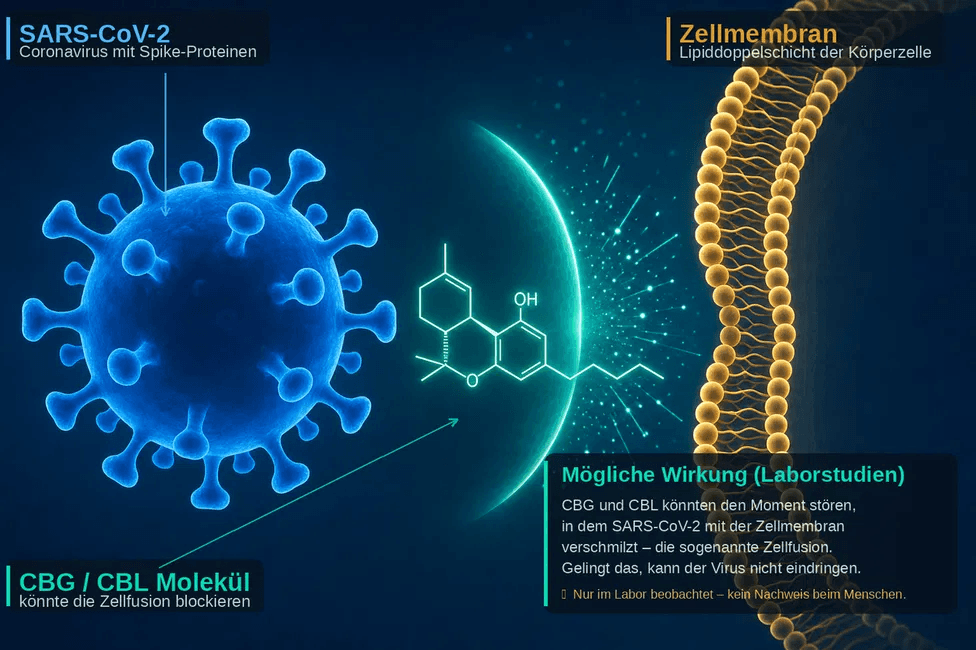
Wichtig:
Alle diese Ergebnisse stammen aus Zellversuchen oder Tiermodellen. Sie beschreiben biologische Mechanismen und keine Behandlungserfolge beim Menschen. Faktoren wie Dosierung, Einnahmeform und der richtige Zeitpunkt spielen eine enorme Rolle. Ein Stoff, der in einer Zellkultur funktioniert, wirkt nicht automatisch genauso beim Menschen (5,6,7).
Wie beeinflussen Cannabinoide starke Entzündungsreaktionen bei COVID-19?
Bei schweren COVID-19-Verläufen ist nicht das Virus allein das Problem – oft ist es die überschießende Reaktion des eigenen Immunsystems, der sogenannte Zytokinsturm (zu Deutsch: eine unkontrollierte Flut von Entzündungsbotenstoffen). Laborversuche zeigen, dass CBD-reiche Extrakte bestimmte dieser Botenstoffe – konkret IL-6 und IL-8 – in Lungenzellkulturen senken können (8).
Allerdings war das Bild nicht einheitlich: In anderen Zelltypen (Makrophagen, also bestimmten Immunzellen) zeigten sich in denselben Versuchen teilweise auch entzündungsfördernde Effekte. Das zeigt, wie komplex das Thema ist – und warum man nicht einfach von „CBD wirkt entzündungshemmend" sprechen kann, ohne den Kontext zu nennen. Belastbare Daten vom Menschen fehlen hier noch vollständig (1,8).
Antiviral oder entzündungshemmend oder beides?
Wahrscheinlich beides – aber je nach Stoff und betrachtetem Mechanismus unterschiedlich. Die in der Pflanze vorkommenden Cannabinoid-Säurevorstufen CBDA und CBGA werden eher mit einer möglichen Blockade des Viruseintritts in Verbindung gebracht. Das Cannabinoid CBD eher mit der Hemmung der Virusvermehrung und der Aktivierung der Immunabwehr. Die Cannabinoide CBG (Cannabigerol) und CBL (Cannabicyclol) eher mit der Störung eines späteren Fusionsschritts (6,7,9).
Erste Laborversuche zeigen außerdem, dass auch Terpene, die aromatischen Begleitstoffe der Cannabispflanze, in Kombination mit CBD eine antivirale und entzündungshemmende Wirkung auf menschliche Coronaviren haben könnten. Diese Daten stammen allerdings aus einem Nischenjournal und sind mit entsprechender Vorsicht zu bewerten (10).
Fazit dieses Abschnitts: Die biologischen Angriffspunkte sind vielseitig und wissenschaftlich ernst zu nehmen. Ein klinischer Beweis beim Menschen fehlt jedoch noch.
Welche Studien gibt es und wie belastbar sind sie?
Um Studienergebnisse einordnen zu können, hilft es, die verschiedenen Arten von Studien zu kennen:
- Laborstudien (In-vitro): Versuche an Zellkulturen. Günstig für erste Hinweise, aber weit entfernt von der Realität im menschlichen Körper. Niedrigste Aussagekraft.
- Tierversuche (In-vivo): Versuche an Tieren. Näher an der menschlichen Biologie, aber nicht direkt übertragbar.
- Klinische Studien: Versuche am Menschen, idealerweise randomisiert, doppelblind und placebokontrolliert (RCT). Das bedeutet: Zufall entscheidet, wer was bekommt; weder Teilnehmende noch Forschende wissen, wer ein Placebo erhält. Höchste Aussagekraft.
- Reviews und Scoping Reviews: Zusammenfassungen vieler Studien. Hilfreich für einen Überblick, aber abhängig von der Qualität der ausgewerteten Einzelstudien.
Der Großteil der verfügbaren Studienlage zu Cannabinoiden und COVID-19 stammt aus Laborstudien (niedrige Aussagekraft). Klinische Daten am Menschen sind wenig vorhanden.

Die bisher einzige methodisch hochwertige klinische Studie ist die CANDIDATE-Studie: Patientinnen und Patienten mit leichtem bis mittelschwerem COVID-19 erhielten 14 Tage lang täglich 300 mg orales CBD, zusätzlich zur Standardversorgung. Das Studiendesign war solide – randomisiert, doppelblind und placebokontrolliert. Die Ergebnisse zeigten keinen klaren klinischen Vorteil: weder bei der Symptomentwicklung noch bei der Verhinderung einer Verschlechterung (5).
Das bedeutet nicht, dass CBD grundsätzlich ohne Wirkung wäre. Es bedeutet, dass diese spezifische Formulierung, Dosierung und Patientengruppe in dieser Studie keinen messbaren Unterschied erzeugt hat. Nachfolgende Übersichtsarbeiten sehen die Datenlage insgesamt als noch nicht ausreichend für eine Therapieempfehlung an (1,2,5).
Was die Forschung zu CBD und Long-COVID-Symptomen untersucht
Long COVID bezeichnet anhaltende Beschwerden nach einer überstandenen COVID-19-Erkrankung – darunter Erschöpfung, Konzentrationsprobleme, Schlafstörungen, Schmerzen und Atembeschwerden, die Wochen oder Monate nach der akuten Infektion fortbestehen. Gesicherte Therapien sind bislang begrenzt (2,11,12).
Forschende untersuchen, ob Cannabinoide bestimmte dieser Symptome begleiten könnten. Das ist ein Forschungsansatz – kein etablierter Behandlungsstandard. Übersichtsarbeiten diskutieren Cannabinoide als möglichen Ansatz, weil Symptome wie Schmerzen, Schlafprobleme und Angst auch in anderen klinischen Zusammenhängen untersucht wurden – nicht nur spekulativ im Long-COVID-Kontext (2,12).

Eine direkte Pilotstudie mit einem CBD-dominanten Produkt bei Long-COVID-Betroffenen zeigte, dass die Anwendung durchführbar war und gut vertragen wurde. Wichtig: Die Studie war sehr klein und hatte keine Vergleichsgruppe. Ein Wirksamkeitsnachweis lässt sich daraus nicht ableiten (11). Pilotdaten dienen dazu, zu prüfen, ob weitere, größere Studien sinnvoll und machbar wären – sie sind kein Beleg für Wirksamkeit.
Wer CBD im Zusammenhang mit Long COVID in Betracht zieht, sollte das unbedingt ärztlich besprechen – nicht zuletzt wegen möglicher Wechselwirkungen mit anderen Medikamenten und der individuellen Situation.
Was du über CBD-Produkte aus dem Handel wissen solltest
Dieser Punkte über CBD-Produkte aus dem Handel sind besonders wichtig, werden aber häufig übersehen:
- Die Cannabinoide, die in wissenschaftlichen Studien eingesetzt werden, sind standardisierte Monosubstanzen (Reinsubstanzen) mit genau definierter Zusammensetzung und Dosierung.
- CBD-Produkte, die frei im Handel erhältlich sind – also Öle, Kapseln oder Cremes sind in der Regel nicht die standardisierte Reinsubstanzen aus den Studien.
- In Deutschland sind frei verkäufliche CBD-Produkte keine Arzneimittel. Das bedeutet: Sie unterliegen nicht denselben strengen Zulassungsanforderungen wie Medikamente, ihre Wirksamkeit wird nicht behördlich geprüft, und sie dürfen offiziell nicht mit dem Anspruch verkauft werden, Krankheiten zu behandeln oder zu heilen.
- Medizinisches Cannabis hingegen, also Cannabis als verschriebenes Arzneimittel, unterliegt anderen rechtlichen Regeln und wird vom Arzt individuell verordnet.
Was das für die Einordnung von Studienergebnissen und Untersuchungen bedeutet: Selbst wenn ein Laborversuch oder eine klinische Studie interessante Ergebnisse für eine bestimmte CBD-Formulierung zeigt, lässt sich daraus kein direkter Rückschluss auf ein frei käufliches Produkt ziehen. Konzentration, Reinheit, Darreichungsform und Begleitstoffe können erheblich variieren und das hat zur Folge, dass auch die Aufnahme im Körper erheblich variieren kann (5,6,11).
Risiken und Nebenwirkungen: Was man zu Cannabinoiden wissen sollte
Auch nicht bewusstseinsverändernde Cannabinoide, wie CBD, sind keine risikofreien Mittel. Wer das weiß, kann fundierter entscheiden.
Bei pharmazeutisch geprüftem CBD – also der in klinischen Studien eingesetzten Monosubstanz – wurden in Studien unter anderem folgende Nebenwirkungen beobachtet: Müdigkeit, verminderter Appetit, Durchfall und vorübergehend erhöhte Leberwerte. Diese Effekte können relevanter werden, wenn Personen bereits andere Medikamente einnehmen oder eine akute Erkrankung den Körper zusätzlich belastet (13).
Beim Thema Wechselwirkungen mit anderen Medikamenten ist besondere Vorsicht angebracht. CBD und THC werden in der Leber über bestimmte Enzyme abgebaut – sogenannte CYP-Enzyme, vor allem CYP3A4. CBD kann dabei die Blutspiegel anderer Wirkstoffe beeinflussen, also dafür sorgen, dass andere Medikamente stärker oder schwächer wirken als gewünscht. Das ist besonders relevant bei:
- Blutverdünnern (z. B. Marcumar, Eliquis)
- Beruhigungs- und Schlafmitteln
- bestimmten Antiepileptika (Medikamenten gegen Epilepsie)
- Paxlovid (einem antiviralen COVID-19-Medikament): Paxlovid enthält Ritonavir, das denselben Leberabbauweg hemmt. Die Kombination kann zu gefährlich veränderten Wirkspiegeln führen (13,14,15).
Was das Rauchen von Cannabis betrifft: Rauch, egal ob von Cannabis oder Tabak, reizt die Atemwege. Bei Husten, Bronchitis oder Atemnot im Rahmen einer COVID-19-Erkrankung kann das bestehende Beschwerden deutlich verschlimmern. Wer Atemwegssymptome hat, sollte vom Konsum in Form von Inhalation dringend absehen (16,17,18).
Wie interagiert Cannabis mit COVID-19-Impfstoffen und Standardtherapien?
Für einen positiven Effekt von Cannabis auf die Wirksamkeit von COVID-19-Impfstoffen gibt es bisher keine überzeugenden Belege. Besser dokumentiert sind dagegen mögliche Wechselwirkungen mit bestimmten Medikamenten – dazu mehr im Abschnitt oben (3,4,19).
Eine kleine Studie untersuchte bei Krebspatientinnen und -patienten mit langjährigem Cannabiskonsum, ob dieser die Antikörperantwort nach einer Booster-Impfung beeinflusst. Ergebnis: kein signifikanter Unterschied. Wegen der sehr kleinen und sehr spezifischen Gruppe, Krebserkrankte mit chronischem Cannabiskonsum, lassen sich aus diesem Befund keine Schlüsse für die Allgemeinbevölkerung ziehen (19).
Cannabinoide im Vergleich mit klassischen COVID-19-Medikamenten
Der wesentliche Unterschied zwischen Cannabinoiden und etablierten COVID-19-Therapeutika liegt nicht in der biologischen Plausibilität, sondern im Stand der klinischen Evidenz – also darin, wie gut die Wirksamkeit beim Menschen belegt ist:
| Therapieansatz | Hauptziel | Evidenz beim Menschen | Einordnung |
| Cannabinoide / Hanf-Extrakte | mögliche antivirale und entzündungshemmende Effekte, evtl. Symptombegleitung | überwiegend Laborstudien, wenig klinische Daten | experimentell, keine Standardtherapie |
| Nirmatrelvir/Ritonavir (Paxlovid) | frühe antivirale Behandlung bei Risikogruppen | leitliniengestützt | relevant in der frühen Phase, aber mit vielen Wechselwirkungen |
| Remdesivir | antivirale Behandlung in ausgewählten Situationen | leitliniengestützt | definierter Einsatz, vor allem bei Risikokonstellationen |
| Dexamethason | Dämpfung überschießender Entzündung | gut belegt bei schwerem COVID-19 | Standard bei schweren Verläufen |
| IL-6-Blocker / weitere Immunmodulatoren | Zusatz bei starker Entzündungsaktivität | leitliniengestützt in ausgewählten schweren Verläufen | gezielter Ergänzungsansatz |
Klassische COVID-19-Medikamente haben ihren Platz nicht deshalb, weil sie „konventionell" sind, sondern weil sie in klinischen Studien mit klaren Endpunkten geprüft wurden. Daran müssen sich auch Cannabinoide messen lassen und genau dort besteht noch erheblicher Forschungsbedarf (3,4).
Fazit
Cannabis und COVID-19 ist ein aktives Forschungsfeld mit interessanten Laborbefunden – aber auch mit noch vielen offenen Fragen. Bestimmte Cannabinoide zeigen in präklinischen Studien antivirale und entzündungshemmende Eigenschaften, die wissenschaftlich ernst genommen werden. Für eine anerkannte COVID-19-Therapie reicht die aktuelle Datenlage nicht aus. Bei Long COVID stehen erste Pilotdaten zur Verfügung, die auf gute Verträglichkeit hindeuten – einen Wirksamkeitsnachweis liefern sie nicht.
Frei käufliche CBD-Produkte sind in Deutschland keine Arzneimittel und dürfen nicht zur Behandlung von Krankheiten eingesetzt werden. Studienergebnisse aus Laborversuchen oder klinischen Studien lassen sich nicht direkt auf diese Produkte übertragen.
Wer sich für Cannabinoide in einem gesundheitlichen Kontext interessiert, sollte das immer als individuelle Entscheidung im ärztlichen Gespräch angehen – informiert, realistisch und mit Blick auf mögliche Wechselwirkungen mit anderen Medikamenten.
Rechtlicher Hinweis
Dieser Artikel dient ausschließlich der allgemeinen Information und ersetzt keine medizinische Beratung. Die Anwendung von Cannabisprodukten zu therapeutischen Zwecken sollte nur in Absprache mit qualifiziertem medizinischem Fachpersonal erfolgen. Es wird keine Haftung für Schäden oder Nebenwirkungen übernommen, die durch unsachgemäßen Gebrauch entstehen können. Weder werden Heil- oder Wirkversprechen gegeben, noch soll die Nutzung ohne ärztlichen Rat angeregt werden. Nutzer sind verpflichtet, die in ihrer Region geltenden gesetzlichen Bestimmungen zu beachten und eigenverantwortlich zu handeln.
Quellen
- Holst, M.; Nowak, D.; Hoch, E. (2022): Cannabidiol As a Treatment for COVID-19 Symptoms? A Critical Review. Cannabis and Cannabinoid Research. DOI: 10.1089/can.2021.0135.
- Scott, C.; Hall, S.; Zhou, J.; Lehmann, C. (2024): Cannabinoids and the Endocannabinoid System in Early SARS-CoV-2 Infection and Long COVID-19—A Scoping Review. Journal of Clinical Medicine 13, 227. DOI: 10.3390/jcm13010227.
- World Health Organization (2025): Therapeutics and COVID-19: living guideline.
- Infectious Diseases Society of America (2025): Guidelines on the Treatment and Management of Patients with COVID-19.
- Crippa, J. A. S. et al. (2022): Cannabidiol for COVID-19 Patients with Mild to Moderate Symptoms (CANDIDATE Study): A Randomized, Double-Blind, Placebo-Controlled Clinical Trial. Cannabis and Cannabinoid Research 7(5), 658–669. DOI: 10.1089/can.2021.0093.
- van Breemen, R. B. et al. (2022): Cannabinoids block cellular entry of SARS-CoV-2 and the emerging variants. Journal of Natural Products 85(1), 176–184. DOI: 10.1021/acs.jnatprod.1c00946.
- Nguyen, L. C. et al. (2022): Cannabidiol inhibits SARS-CoV-2 replication through induction of the host ER stress and innate immune responses. Science Advances 8(8), eabi6110. DOI: 10.1126/sciadv.abi6110.
- Anis, O. et al. (2021): Cannabis compounds exhibit anti-inflammatory activity in vitro in COVID-19-related inflammation in lung epithelial cells and pro-inflammatory activity in macrophages. Scientific Reports 11, 1462. DOI: 10.1038/s41598-021-81049-2.
- Classen, N. et al. (2024): Cannabigerol and Cannabicyclol Block SARS-CoV-2 Cell Fusion. Planta Medica 90(9), 717–725. DOI: 10.1055/a-2320-8822.
- Chatow, L. et al. (2024): Terpenes and cannabidiol against human corona and influenza viruses—Anti-inflammatory and antiviral in vitro evaluation. Biotechnology Reports 41, e00829. DOI: 10.1016/j.btre.2024.e00829.
- Thurgur, H.; Lynskey, M.; Schlag, A. K.; Croser, C.; Nutt, D. J.; Iveson, E. (2024): Feasibility of a cannabidiol-dominant cannabis-based medicinal product for the treatment of long COVID symptoms: A single-arm open-label feasibility trial. British Journal of Clinical Pharmacology. DOI: 10.1111/bcp.15988.
- Cárdenas-Rodríguez, N. et al. (2024): Possible Role of Cannabis in the Management of Neuroinflammation in Patients with Post-COVID Condition. International Journal of Molecular Sciences 25(7), 3805. DOI: 10.3390/ijms25073805.
- U.S. Food and Drug Administration (2025): EPIDIOLEX prescribing information / label.
- Antoniou, T.; Bodkin, J.; Ho, J. M.-W. (2020): Drug interactions with cannabinoids. CMAJ 192(9), E206. DOI: 10.1503/cmaj.191097.
- U.S. Food and Drug Administration (2024): PAXLOVID full prescribing information / label.
- Griffith, N. B. et al. (2024): Cannabis, Tobacco Use, and COVID-19 Outcomes. JAMA Network Open 7(6), e2417977. DOI: 10.1001/jamanetworkopen.2024.17977.
- Huang, J.; Xu, Y.; Na, M. (2022): Cannabis Use Is Associated With Lower COVID-19 Susceptibility but Poorer Survival. Frontiers in Public Health 10, 829715. DOI: 10.3389/fpubh.2022.829715.
- Kaplan, A. G. (2021): Cannabis and Lung Health: Does the Bad Outweigh the Good? Pulmonary Therapy 7(2), 395–408. DOI: 10.1007/s41030-021-00171-8.
- Cohen Idan, C. et al. (2022): Evaluation of immune response to anti-COVID-19 booster in cancer patients and chronic medical cannabis users. Cancer Communications 42(12), 1417–1420. DOI: 10.1002/cac2.12353.